À propos du produit
Le fruit d'Amla est une ancienne source alimentaire utilisée depuis des siècles en médecine ayurvédique.
Il est originaire du sous-continent indien et fait partie intégrante de l’alimentation traditionnelle indienne. Le fruit de l'amla est petit, rond et jaune-vert. Il a un goût aigre-doux et est souvent utilisé en cuisine ou comme collation.
Le fruit a une haute valeur nutritionnelle et est utilisé en médecine traditionnelle pour diverses affections.
Aujourd’hui, l’amla est largement utilisée comme ingrédient dans de nombreux produits de santé et est souvent incluse dans les tisanes et les jus.
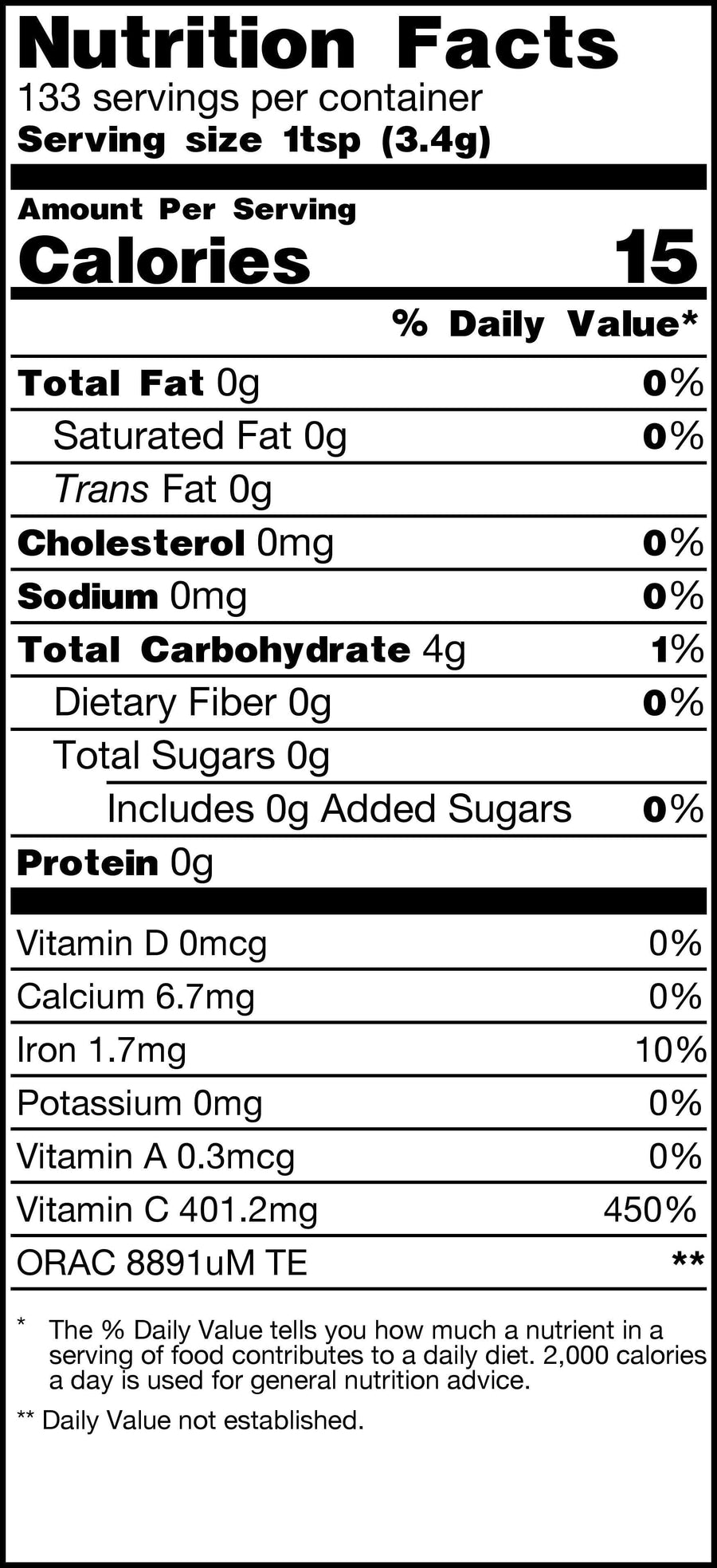
Nutriments puissants dans notre poudre de fruits frais et bio Amla
-
Acides gras : linoléique, linolénique, oléique, stéarique, palmitique.
-
Vitamines : Vitamine C, Fer
Phytochimiques : terpénoïdes, alcaloïdes, flavonoïdes, tanins hydrolysables (emblicanine A, emblicanine B, pédonculagine), acide gallique, acide ellagique, 1-Ogalloyl-bêta-D-glucose, 3, 6-di-O--D-glucose, acide , quercétine, corilagine, lupéol
Le goût, l'odeur, la texture et la couleur varient d'un lot à l'autre. En raison de sa nature, cette poudre a tendance à s'agglutiner. En cas d'agglutination, posez le sac sur une surface plane et placez une serviette sur le sac. Frappez ensuite sur le sac jusqu'à ce que les mottes se brisent. La serviette aidera à protéger le sac contre les dommages.
Utilisation suggérée : Mélangez 1 cuillère à café avec du jus et du yogourt, ou ajoutez-le à votre smoothie préféré.
Suggestion de mélange : Pour augmenter la saveur et le profil nutritionnel, combiné avec nos poudres biologiques de cerise acérola et d'églantier.
Faits divers sur notre poudre d'amla biologique
Certifications : Certifié biologique USDA.
Ingrédients : Fruit d'Amla cru.
Parties utilisées : Amla entière, sans graine.
Nom botanique : Emblica Officinalis.
Autres noms : Amalaki, groseille indienne.
Origine : Cultivé et séché en Inde et conditionné avec soin en Floride, aux États-Unis.
Comment maintenir une fraîcheur optimale
- Ce produit est emballé dans des sachets en aluminium hermétiques et refermables pour une fraîcheur optimale.
- Une fois ouvert, poussez l'air hors du sachet avant de le refermer pour préserver une puissance maximale.
- Conservez votre poudre dans un endroit frais, sombre et sec.
Ce produit est 100% naturel et peu transformé :
Le goût, l'odeur, la texture et la couleur varient d'un lot à l'autre. Rendez-vous ici pour savoir pourquoi nos produits peuvent naturellement varier.
Les protections importantes que nous prenons pour vous apporter des superaliments sûrs et nutritifs :
Veuillez vous rendre ici pour découvrir les mesures essentielles que nous prenons pour fournir une nutrition fraîche et de qualité.
Quantités en vrac ?
Besoin de commander une grande quantité de nos produits ? Nous sommes heureux de vous aider! Veuillez contacter notre département Vrac pour discuter des détails.
* L'emballage du produit, les images et l'origine peuvent varier.
Sources & References
1. Médecine ayurvédique d’Inde. (2020). "Amla en médecine ayurvédique."
2. NIH. (2019). «Potentiel phytochimique et thérapeutique de l'Amla».
3. Programmes de recherche clinique de la Harvard Medical School. (2021). "Propriétés antioxydantes de l'Amla."
4. QUI. (2020). «Amla et santé immunitaire».
5. Principes de l'herboristerie orientale. (2021). «Amla en phytothérapie orientale».
6. Principes de l'herboristerie occidentale. (2022). «Avantages cardiovasculaires d'Amla».
7. Médecine traditionnelle chinoise. (2021). "Amla en MTC."
8. FDA. (2021). "Applications cosmétiques d'Amla."
9. Centre d'information sur la recherche de la clinique Mayo. (2019). «Bénéfices dermatologiques de l'Amla».
10. USDA. (2020). "Culture durable de l'Amla."
11. Recherche scientifique dans l'ex-Union soviétique. (2020). "Propriétés anticancérigènes de l'Amla."
12. QUI. (2021). "Contenu en vitamine C dans Amla."
13. Rege NN, Thatte UM, Dahanukar SA. Propriétés adaptogènes de six herbes rasayana utilisées en médecine ayurvédique. Phytother Rés. 1999 juin ; 13(4) : 275-91.
14. Kumar KS, Muller K. Plantes médicinales du Népal ; II. Évaluation comme inhibiteurs de la peroxydation lipidique dans les membranes biologiques. J Ethnopharmacol. 1999 février ; 64(2) : 135-9.
15. Sabu MC, Kuttan R. Activité antidiabétique des plantes médicinales et sa relation avec leur propriété antioxydante. J Ethnopharmacol. Juillet 2002;81(2):155-60.
16. Augusti KT, Arathy SL, Asha R et al. Une étude comparative sur les effets bénéfiques de l'ail (Allium sativum Linn), de l'amla (Emblica Officinalis Gaertn) et de l'oignon (Allium cepa Linn) sur l'hyperlipidémie induite par la graisse de beurre et la graisse de bœuf chez le rat. Indien J Exp Biol. Août 2001;39(8):760-6.
17. Anila L, Vijayalakshmi NR. Flavonoïdes d'Emblica officinalis et de Mangifera indica-efficacité contre la dyslipidémie. J Ethnopharmacol. janvier 2002;79(1):81-7.
18. Kim HJ, Yokozawa T, Kim HY et al. Influence de l'amla (Emblica officinalis Gaertn.) sur l'hypercholestérolémie et la peroxydation lipidique chez les rats nourris avec du cholestérol. J Nutr Sci Vitaminol (Tokyo). décembre 2005;51(6):413-8.
19. Saravanan S, Srikumar R, Manikandan S, Jeya PN, Sheela DR. Effet hypolipidémique du triphala chez des rats hypercholestérolémiques induits expérimentalement. Yakugaku Zasshi. Février 2007;127(2):385-8.
20. Rao TP, Sakaguchi N, Juneja LR, Wada E, Yokozawa T. Les extraits d'Amla (Emblica officinalis Gaertn.) réduisent le stress oxydatif chez les rats diabétiques induits par la streptozotocine. J Med Nourriture. 2005;8(3):362-8.
21. Gao X, Zhang H, Schmidt AM, Zhang C. AGE/RAGE produit un dysfonctionnement endothélial dans les artérioles coronaires chez les souris diabétiques de type 2. Am J Physiol Coeur Circ Physiol. Août 2008 ; 295(2) :H491-8.
22. Su J, Lucchesi PA, Gonzalez-Villalobos RA et al. Rôle des produits finaux de glycation avancée avec stress oxydatif dans le dysfonctionnement des artères de résistance chez les souris diabétiques de type 2. Artériosclér Thromb Vasc Biol. Août 2008;28(8):1432-8.
23. Stirban A, Negrean M, Gotting C et al. Produits finaux alimentaires avancés de glycation et stress oxydatif : effets in vivo sur la fonction endothéliale et les adipokines. Ann NY Acad Sci. avril 2008 ; 1126 : 276-9.
24. Smit AJ, Hartog JW, Voors AA, van Veldhuisen DJ. Produits finaux avancés de glycation dans l’insuffisance cardiaque chronique. Ann NY Acad Sci. avril 2008 ; 1126 : 225-30.
25. Ramasamy R, Yan SF, Herold K, Clynes R, Schmidt AM. Récepteur des produits finaux de glycation avancée : rôles fondamentaux dans la réponse inflammatoire : ouvrir la voie à la pathogenèse du dysfonctionnement endothélial et de l'athérosclérose. Ann NY Acad Sci. Avril 2008 ; 1126 : 7-13.
26. Bhattacharya SK, Bhattacharya A, Sairam K, Ghosal S. Effet des principes tannoïdes bioactifs d'Emblica officinalis sur le stress oxydatif induit par l'ischémie-reperfusion dans le cœur de rat. Phytomédecine. mars 2002;9(2):171-4.
27. Antony B, Merina B, Sheeba V, Mukkadan J. Effet de l'extrait d'Amla standardisé sur l'athérosclérose et la dyslipidémie. Indien J Pharm Sci. 2006;68(4):437-41.
28. Mathur R, Sharma A, Dixit VP, Varma M. Effet hypolipidémique du jus de fruit d'Emblica officinalis chez des lapins nourris au cholestérol. J Ethnopharmacol. 1996 février ; 50(2) :61-8.
29. Duan W, Yu Y, Zhang L. Effets antiathérogènes du phyllanthus emblica associés à la corilagin et à son analogue. Yakugaku Zasshi. Juillet 2005;125(7):587-91.
30. Yokozawa T, Kim HY, Kim HJ, Okubo T, Chu DC, Juneja LR. Amla (Emblica officinalis Gaertn.) prévient la dyslipidémie et le stress oxydatif dans le processus de vieillissement. F. J Nutr. juin 2007;97(6):1187-95.
31. Cai X. Régulation des cellules musculaires lisses dans le développement et les maladies vasculaires : stratégies thérapeutiques actuelles. Expert Rév Cardiovasc Ther. 2006 novembre;4(6):789-800.
32. Lembo G, Vecchione C, Morisco C et al. Hypertension artérielle et athérosclérose : leur épidémiologie et physiopathologie. Ann Ital Med Int. 1995 octobre ; 10 Suppl : 69S-72S.
33. Jacob A, Pandey M, Kapoor S, Saroja R. Effet de la groseille indienne (amla) sur les taux de cholestérol sérique chez les hommes âgés de 35 à 55 ans. Eur J Clin Nutr. 1988 novembre ; 42(11) : 939-44.
34. Manjunatha S, Jaryal AK, Bijlani RL, Sachdeva U, Gupta SK. Effet du Chyawanprash et de la vitamine C sur la tolérance au glucose et le profil lipoprotéique. Indien J Physiol Pharmacol. janvier 2001;45(1):71-9.
35. Nissen SE, Nicholls SJ, Wolski K et al. Effets d'un agoniste PPAR-alpha puissant et sélectif chez les patients atteints de dyslipidémie athérogène ou d'hypercholestérolémie : deux essais contrôlés randomisés. JAMA. 28 mars 2007; 297(12):1362-73.
36. Laboratoire de R&D, Arjuna Natural Extracts Ltd PBNO 126 Alwaya Cohin Karala Inde. Réduction du risque de maladie coronarienne (CHD) grâce à un ciblage multi-composants, y compris les niveaux de CRP en utilisant Amlamax' (AED-205), l'extrait sec standardisé d'Emblica officianalis Gaertn. (Groseille indienne). 2007.
37. Laboratoire de R&D, Arjuna Natural Extracts Ltd PBNO 126 Alwaya Cohin Karala Inde. Amlama dans la gestion de la dyslipidémie chez l'homme. 2007
38. Dilaveris P, Giannopoulos G, Riga M, Synetos A, Stefanadis C. Effets bénéfiques des statines sur le dysfonctionnement endothélial et la raideur vasculaire. Curr Vasc Pharmacol. Juillet 2007;5(3):227-37.
39. Kazi D, Farmer JA. Augmenter le cholestérol des lipoprotéines de haute densité : stratégies innovantes contre un vieil adversaire. Curr Atheroscler Rep. 2005 mars; 7 (2): 88-94.
40. Paragh G, Seres I, Harangi M et al. Le ciprofibrate augmente l'activité paraoxonase chez les patients atteints du syndrome métabolique. Br. J Clin Pharmacol. juin 2006;61(6):694-701.
41. Tomas M, Latorre G, Senti M, Marrugat J. La fonction antioxydante des lipoprotéines de haute densité : un nouveau paradigme dans l'athérosclérose. Révérend Esp Cardiol. Juin 2004;57(6):557-69.
42. Mackness MI, Durrington PN, Mackness B. Le rôle de l'activité paraoxonase 1 dans les maladies cardiovasculaires : potentiel d'intervention thérapeutique. Suis J Médicaments Cardiovasc. 2004;4(4):211-7.
43. Costa LG, Vitalone A, Cole TB, Furlong CE. Modulation de l'activité paraoxonase (PON1). Biochem Pharmacol. 15 février 2005;69(4):541-50.
44. Dantoine T, Debord J, Merle L, Charmes JP. De la toxicité des composés organophosphorés à l'athérosclérose : rôle de la paraoxonase 1. Rev Med Interne. Juillet 2003;24(7):436-42.
45. van Himbergen TM, van Tits LJ, Roest M, Stalenhoef AF. L’histoire de PON1 : comment une enzyme hydrolysant les organophosphorés devient un acteur incontournable en médecine cardiovasculaire. Neth J Med. Février 2006 ; 64(2) :34-8.
46. Mackness B, Hine D, Liu Y, Mastorikou M, Mackness M. La paraoxonase-1 inhibe la production de MCP-1 induite par les LDL oxydées par les cellules endothéliales. Biochem Biophys Res Commun. 4 juin 2004;318(3):680-3.
47. Aviram M, Kaplan M, Rosenblat M, Fuhrman B. Antioxydants alimentaires et paraoxonases contre l'oxydation des LDL et le développement de l'athérosclérose. Handb Exp Pharmacol. 2005;(170):263-300.
48. Graner M, James RW, Kahri J et al. Association de l'activité et de la concentration de la paraoxonase-1 avec la gravité angiographique et l'étendue de la maladie coronarienne. J Am Coll Cardiol. 20 juin 2006;47(12):2429-35.
49. Marchegiani F, Marra M, Spazzafumo L et al. L'activité paraoxonase et le génotype prédisposent à un vieillissement réussi. J Gérontol A Biol Sci Med Sci. juin 2006;61(6):541-6.
50. Barter PJ, Kastelein JJ. Cibler la protéine de transfert des esters de cholestérol pour la prévention et la gestion des maladies cardiovasculaires. J Am Coll Cardiol. 7 février 2006;47(3):492-9.
51. Morton RE, Greene DJ. La suppression partielle de l'activité de la CETP modifie de manière bénéfique le profil de transfert lipidique du plasma. Athérosclérose. Mai 2007 ; 192(1) : 100-7.
52. Hayes JD, Kelleher MO, Eggleston IM. Les actions chimiopréventives contre le cancer des composés phytochimiques dérivés des glucosinolates. Eur J Nutr. Mai 2008 ; 47 Supplément 2 : 73-88.
53. Mukherjee S, Gangopadhyay H, Das DK. Brocoli : un légume unique qui protège le cœur des mammifères grâce au cycle rédox de la superfamille des thiorédoxines. J Agric Food Chem. 23 janvier 2008;56(2):609-17.
54. Zhu H, Jia Z, Strobl JS et al. Puissante induction d'antioxydants cellulaires et mitochondriaux totaux et d'enzymes de phase 2 par le sulforaphane crucifère dans les cellules musculaires lisses de l'aorte de rat : cytoprotection contre le stress oxydatif et électrophile. Toxicol cardiovasculaire. 8 juillet 2008.
55. Baek SH, Park M, Suh JH, Choi HS. Effets protecteurs d'un extrait de jeune radis (Raphanus sativus L) cultivé avec du soufre (extrait de radis soufré) et du sulforaphane sur l'hépatotoxicité induite par le tétrachlorure de carbone. Biosci Biotechnologie Biochem. 2008 mai ; 72(5) : 1176-82.
56. Tiku AB, Abraham SK, Kale RK. Effet protecteur de la feuille de moutarde végétale crucifère (Brassica campestris) contre les dommages chromosomiques in vivo et le stress oxydatif induits par les rayonnements gamma et les produits chimiques génotoxiques. Environ Mol Mutagène. Juin 2008;49(5):335-42.
57. Dinkova-Kostova AT, Fahey JW, et al. Induction de la réponse de phase 2 dans la peau de souris et humaine par des extraits de pousses de brocoli contenant du sulforaphane. Biomarqueurs épidémiologiques du cancer Précédent. avril 2007;16(4):847-51.
58. Wu L, Noyan Ashraf MH, Facci M et al. Approche diététique pour atténuer le stress oxydatif, l’hypertension et l’inflammation du système cardiovasculaire. Proc Natl Acad Sci USA. 4 mai 2004;101(18):7094-9.
59. Département R&D, VDF FutureCeuticals. Mélange de graines crucifères germées, SproutGarden, augmente les taux sanguins de HDL. 2008.
60. Département R&D, VDF FutureCeuticals. Effet inhibiteur de longue durée du mélange de graines de crucifères germées sur l'oxydation des LDL induite par le Cu ex vivo. 2008.
61. Département R&D, VDF FutureCeuticals. Le mélange de graines crucifères germées, SproutGarden, réduit les taux sanguins d'oxLDL. 2008.
62. Département R&D, VDF FutureCeuticals. SproutGarden (#1) stimule l'activité de la Paraoxonase 1 dans le sang humain. Cas d’effet aigu.
63. Département R&D, VDF FutureCeuticals. SproutGarden-C inhibe l'activité de la protéine de transfert d'ester de cholestérol (CETP) in vivo. Étude de cas clinique aigu. 2008.
64. Département R&D, VDF FutureCeuticals. SproutGarden-C inhibe l'activité de la protéine de transfert d'ester de cholestérol (CETP) in vivo. Étude de cas clinique aigu. 2008.
65. Sigal LH. Science fondamentale pour le clinicien 44 : athérosclérose : une maladie à médiation immunologique (auto-immune ?). J Clin Rheumatol. Juin 2007;13(3):160-8.
66. Liang CP, Han S, Senokuchi T, Tall AR. Le macrophage au carrefour de la résistance à l’insuline et de l’athérosclérose. Circ Rés. 8 juin 2007;100(11):1546-55.
67. Ferri C, Croce G, Cofini V et al. Protéine C-réactive : interaction avec l'endothélium vasculaire et rôle possible dans l'athérosclérose humaine. Curr Pharm Des. 2007;13(16):1631-45.
68. Martins e Silva, Saldanha C. Régime alimentaire, athérosclérose et événements athérothrombotiques. Révérend Port Cardiol. mars 2007;26(3):277-94.
69. Coppola G, Novo S. Statines et maladie artérielle périphérique : effets sur la claudication, la progression de la maladie et la prévention des événements cardiovasculaires. Arch Med Rés. Juillet 2007;38(5):479-88.
70. Jain RK, Finn AV, Kolodgie FD, Gold HK, Virmani R. Thérapie antiangiogénique pour la normalisation du système vasculaire de la plaque athéroscléreuse : une stratégie potentielle pour la stabilisation de la plaque. Nat Clin Pract Cardiovasc Med. Septembre 2007;4(9):491-502.
71. Singh IM, Shishehbor MH, Ansell BJ. Les lipoprotéines de haute densité comme cible thérapeutique : une revue systématique. JAMA. 15 août 2007; 298(7):786-98.
72. Windler E, Schoffauer M, Zyriax BC. L'importance de faibles niveaux de cholestérol HDL dans une société vieillissante présentant un risque accru de maladies cardiovasculaires. Diab Vasc Dis Res. Juin 2007;4(2):136-42.
73. Jacobson TA, Miller M, Schaefer EJ. Hypertriglycéridémie et réduction du risque cardiovasculaire. Clin Ther. 2007 mai ; 29(5) : 763-77.
74. Rivera JJ, Blumenthal RS, Ashen D. Cholestérol à lipoprotéines de basse densité chez les individus asymptomatiques à haut risque. J Cardiometab Syndr. 2007;2(1):49-52.
75. Libby P. La majorité oubliée : un travail inachevé en matière de réduction du risque cardiovasculaire. J Am Coll Cardiol. 4 octobre 2005;46(7):1225-8.
76. Ali R, Alexander KP. Statines pour la prévention primaire des événements cardiovasculaires chez les personnes âgées : une revue des données probantes. Suis J Geriatr Pharmacother. mars 2007;5(1):52-63.
77. Kunte H, Amberger N, Ruckert RI, Harms L. Statines et leur influence sur les processus inflammatoires dans la sténose de l'artère carotide interne. Zentralbl Chir. Juin 2007;132(3):193-7.
78. Troc PJ, Rye KA. Les fibrates ont-ils un rôle dans la prise en charge de la dyslipidémie dans le syndrome métabolique ? Artériosclér Thromb Vasc Biol. 2008 janvier ; 28(1):39-46.
79. Doncheva NI, Nikolov KV, Vassileva DP. Effets lipidiques et pléiotropes du gemfibrozil, de la simvastatine et de la pravastatine chez les patients atteints de dyslipidémie. Folia Med (Plovdiv). 2006;48(3-4):56-61.
80. Vaverkova H. Double inhibition du cholestérol à l'aide de l'association médicamenteuse ézétimibe/simvastatine ? Vnitr Lek. avril 2007;53(4):421-7.
81. Bhatt DL. Les agents anti-inflammatoires et les antioxydants comme possible « troisième grande vague » en prévention secondaire cardiovasculaire. Je suis J Cardiol. 22 mai 2008;101(10A):4D-13D.
82. Fedoruk LM, Wang H, Conaway MR, Kron IL, Johnston KC. Le traitement par statines améliore les résultats après une chirurgie valvulaire cardiaque. Ann Thorac Chirurgie. Mai 2008 ; 85(5) : 1521-5 ; discussion 1525-6.
83. Graf K, Dietrich T, Tachezy M et al. Surveillance de l'intervention thérapeutique avec l'ézétimibe à l'aide d'une imagerie par fluorescence proche infrarouge ciblée dans l'athérosclérose expérimentale. Imagerie Mol. 2008 mars-avril;7(2):68-76.
84. Scheen AJ, Radermecker RP. Drogue du mois. Comprimé d'ézétimibe/simvastatine (Inegy). Révérend Med Liège. Septembre 2007;62(9):585-90.
85. Stroup J, Stephens J. Produits médicamenteux combinés : une indication pour le bilan comparatif des médicaments et les conseils du pharmacien. J Am Pharm Assoc (2003). 2008 juillet-août ; 48(4) :541-3.
86. Disponible sur : http://www.fda.gov/cder/drug/early_comm/ezetimibe_simvastatin_SEAS.htm. Consulté le 9 septembre 2008.
87. Disponible sur : http://www.fda.gov/Cder/drug/InfoSheets/HCP/simvastatin_amiodaroneHCP.htm. Consulté le 9 septembre 2008.
88. Franceschi C, Bonafe M. Les centenaires comme modèle pour vieillir en bonne santé. Biochem Soc Trans. 2003 avril ; 31(2) : 457-61.
89. Manjunatha S, Jaryal AK, Bijlani RL, Sachdeva U, Gupta SK. Effet du chyawanprash et de la vitamine C sur la tolérance au glucose et le profil lipoprotéique. Indien J Physiol Pharmacol. janvier 2001;45(1):71-9.
90. Aneja R, Odoms K, Denenberg AG, Wong HR. La théaflavine, un extrait de thé noir, est un nouveau composé anti-inflammatoire. Soins critiques Med. 2004 octobre ; 32(10) : 2097-103.
91. Ridker PM, Danielson E, Fonseca FA et al. Rosuvastatine pour prévenir les événements vasculaires chez les hommes et les femmes présentant une protéine C-réactive élevée. N Engl J Med. 9 novembre 2008.
92. Franceschi C. L'inflammation comme caractéristique majeure des personnes âgées : peut-elle être prévenue ou guérie ? Nutr Rev.2007 décembre;65(12 Pt 2):S173-6.
93. Mach F. L'inflammation est une caractéristique cruciale de l'athérosclérose et une cible potentielle pour réduire les événements cardiovasculaires. Handb Exp Pharmacol. 2005;(170):697-722.
94. Fillit HM, Butler RN, O"'Connell AW, et al. Atteindre et maintenir la vitalité cognitive avec le vieillissement. Mayo Clin Proc. 2002 Jul;77(7):681-96.
95. Mishto M, Santoro A, Bellavista E et al. Immunoprotéasomes et immunosénescence. Aging Res Rev. 2003 octobre;2(4):419-32.
96. Giunta S. L'inflammation est-elle un syndrome subclinique d'immunité auto[innée] ? Vieillissement immunitaire. 2006;312.
97. Franceschi C, Capri M, Monti D et al. Inflammatoire et anti-inflammatoire : une perspective systémique sur le vieillissement et la longévité a émergé d’études chez l’homme. Développeur Mech Aging. janvier 2007;128(1):92-105.
98. Florez H, Troen BR. Graisse et inflammation : une double voie vers l’inaptitude chez les personnes âgées ? J Am Geriatr Soc. mars 2008;56(3):558-60.
99. Forte GI, Cala C, Scola L et al. Rôle de l'interaction des facteurs environnementaux et génétiques dans le développement des maladies liées à l'âge : le paradigme du cancer gastrique. Rajeunissement Rés. 2008 avril ; 11 (2) : 509-12.
100. Katepalli MP, Adams AA, Lear TL, Horohov DW. L'effet de l'âge et de la longueur des télomères sur la fonction immunitaire du cheval. Dev Comp Immunol. 2008;32(12):1409-15.
101. Belluck P. Les médicaments anti-cholestérol présentent des avantages plus larges. Le New York Times. 10 novembre 2008;A1.
102. Escobar C, Echarri R, Barrios V. Profils de sécurité relatifs des schémas thérapeutiques à haute dose de statines. Gestion des risques sanitaires Vasc. 2008;4(3):525-33.
103. Beltz LA, Bayer DK, Moss AL, Simet IM. Mécanismes de prévention du cancer par les polyphénols du thé vert et noir. Agents anticancéreux Med Chem. Septembre 2006;6(5):389-406.
104. Cameron AR, Anton S, Melville L et al. Les polyphénols du thé noir imitent la signalisation de l'insuline/du facteur de croissance analogue à l'insuline-1 au facteur de longévité FOXO1a. Cellule vieillissante. 2008 janvier ; 7(1) :69-77.
105. Fernandes G. Progrès en immunologie nutritionnelle. Immunol Rés. 2008;40(3):244-61.
106. Kussmann M, Blum S. Cibles dérivées de l'OMICS pour les troubles inflammatoires de l'intestin : opportunités pour le développement de biomarqueurs liés à la nutrition. Cibles des médicaments contre les troubles immunitaires Endocr Metab. décembre 2007;7(4):271-87.
107. Caramia G. Oméga-3 : de l'huile de foie de morue à la nutrigénomique. Minerva Pédiatre. Août 2008;60(4):443-55.
108. Crujeiras AB, Parra D, Milagro FI et al. Expression différentielle des gènes liés au stress oxydatif et à l'inflammation dans les cellules mononucléées du sang périphérique en réponse à un régime hypocalorique : une étude nutrigénomique. OMICS. 7 août 2008.
109. Gillies PJ. Nutrition préventive des états pro-inflammatoires : un modèle nutrigénomique. Nutr Rev.2007 décembre;65(12 Pt 2):S217-20.
110. Lindi V, Schwab U, Louheranta A et al. Impact du polymorphisme Pro12Ala du gène PPAR-gamma2 sur la réponse sérique des triacylglycérols à la supplémentation en acides gras n-3. Mol Genet Métab. Mai 2003 ; 79(1) :52-60.
111. Tsitouras PD, Gucciardo F, Salbe AD, Heward C, Harman SM. Un apport élevé en graisses oméga-3 améliore la sensibilité à l’insuline et réduit la CRP et l’IL6, mais n’affecte pas les autres axes endocriniens chez les personnes âgées en bonne santé. Horm Metab Res. mars 2008;40(3):199-205.
112. Blazovics A, Hagymasi K, Pronai L. Cytokines, prostaglandines, facteurs nutritifs et non nutritifs dans les maladies inflammatoires de l'intestin. Orv Hétil. 12 décembre 2004;145(50):2523-9.
113. Chen HW, Lee JY, Huang JY et al. La curcumine inhibe l’invasion des cellules cancéreuses du poumon et les métastases via le suppresseur de tumeur HLJ1. Cancer Rés. 15 septembre 2008;68(18):7428-38.
114. Maron DJ, Lu GP, Cai NS et al. Effet hypocholestérolémiant d'un extrait de thé vert enrichi en théaflavine : un essai contrôlé randomisé. Arch Intern Med. 23 juin 2003;163(12):1448-53.
115. Duffy SJ, Keaney JF, Jr., Holbrook M et al. La consommation de thé noir à court et à long terme inverse le dysfonctionnement endothélial chez les patients atteints de maladie coronarienne. Circulation. 10 juillet 2001;104(2):151-6.
116. Kebschull M, Demmer R, Behle JH et al. La protéine chimiotactique 2 des granulocytes (gcp-2/cxcl6) complète l'interleukine-8 dans les maladies parodontales. J Res. Parodontale. 7 octobre 2008.
117. Higashimoto Y, Yamagata Y, Taya S et al. Inflammation systémique dans la BPCO et l'asthme : similitudes et différences. Nihon Kokyuki Gakkai Zasshi. Juin 2008;46(6):443-7.
118. Aukrust P, Yndestad A, Smith C, Ueland T, Gullestad L, Damas JK. Les chimiokines dans la prédiction du risque cardiovasculaire. Thromb Hémostique. 2007 mai ;97(5):748-54.
119. Steptoe A, Gibson EL, Vuononvirta R et al. Les effets de la consommation chronique de thé sur l'activation et l'inflammation des plaquettes : un essai en double aveugle contrôlé par placebo. Athérosclérose. Août 2007;193(2):277-82.
120. Sugatani J, Fukazawa N, Ujihara K et al. Les polyphénols du thé inhibent l'acétyl-CoA:1-alkyl-sn-glycéro-3-phosphocholine acétyltransférase (une enzyme clé dans la biosynthèse du facteur d'activation plaquettaire) et l'agrégation plaquettaire induite par le facteur d'activation plaquettaire. Int Arch Allergie Immunol. Mai 2004 ; 134(1) :17-28.
121. Cai F, Li CR, Wu JL et al. La théaflavine améliore les lésions d'ischémie-reperfusion cérébrale chez le rat grâce à son effet anti-inflammatoire et à la modulation de STAT-1. Médiateurs Inflamm. 2006;2006(5):30490.
122. Siddiqui IA, Adhami VM, Afaq F, Ahmad N, Mukhtar H. Modulation des voies de la phosphatidylinositol-3-kinase/protéine kinase B et de la protéine kinase activée par un mitogène par les polyphénols du thé dans les cellules cancéreuses de la prostate humaine. J Cell Biochimie. 1er février 2004;91(2):232-42.
123. Siddiqui IA, Raisuddin S, Shukla Y. Effets protecteurs de l'extrait de thé noir sur les dommages oxydatifs induits par la testostérone dans la prostate. Cancer Lett. 28 septembre 2005;227(2):125-32.
124. Siddiqui IA, Zaman N, Aziz MH, et al. Inhibition de la croissance tumorale CWR22Rnu1 et de la sécrétion de PSA chez des souris nues athymiques par les thés verts et noirs. Carcinogenèse. avril 2006;27(4):833-9.
125. Zykova TA, Zhang Y, Zhu F, Bode AM, Dong Z. Les réseaux de transduction de signaux requis pour la phosphorylation de STAT1 à Ser727 dans les cellules JB6 épidermiques de souris dans la réponse UVB et les mécanismes inhibiteurs des polyphénols du thé. Carcinogenèse. Février 2005 ; 26(2) : 331-42.
126. Disponible sur : http://www.medicalnewstoday.com/articles/67591.php. Consulté le 23 octobre 2008.
127. WG0401 protège contre l’inflammation généralisée dans une étude humaine. Données non publiées, WellGen, Inc ; 2007.
128. McGuirk P, Higgins SC, Mills KH. Cellules régulatrices et contrôle des infections respiratoires. Curr Allergy Asthma Rep. 2005 janvier;5(1):51-5.
129. Dreger H, Lorenz M, Kehrer A, Baumann G, Stangl K, Stangl V. Caractéristiques de la cardioprotection médiée par la catéchine et la théaflavine. Exp Biol Med (Maywood). avril 2008;233(4):427-33.
130. Jochmann N, Lorenz M, Krosigk A et al. L’efficacité du thé noir pour améliorer la fonction endothéliale est équivalente à celle du thé vert. F. J Nutr. avril 2008;99(4):863-8.
131. Scartezzini P, Speroni E. Revue de certaines plantes de médecine traditionnelle indienne à activité antioxydante. J Ethnopharmacol. Juillet 2000;71(1-2):23-43.
132. Satiavati GV. L'héritage de caraka (critique de livre). Science actuelle. 2003;85 : 1087-90.
133. Damodaran M, Nair KR. Un tanin issu de la groseille indienne (Phyllanthus emblica) à action protectrice sur l'acide ascorbique. Biochem J. 1936 juin; 30 (6): 1014-20.
134. Bhattacharya A, Chatterjee A, Ghosal S, Bhattacharya SK. Activité antioxydante des principes tannoïdes actifs d'Emblica officinalis (amla). Indien J Exp Biol. Juillet 1999;37(7):676-80.
135. Kumar KS, Muller K. Plantes médicinales du Népal ; II. Évaluation comme inhibiteurs de la peroxydation lipidique dans les membranes biologiques. J Ethnopharmacol. 1999 février ; 64(2) : 135-9.
136. Yokozawa T, Kim HY, Kim HJ et al. Amla (Emblica officinalis Gaertn.) atténue le dysfonctionnement rénal lié à l'âge par le stress oxydatif. J Agric Food Chem. 19 septembre 2007;55(19):7744-52.
137. Monnier VM, Mustata GT, Biemel KL, et al. "Réticulation de la matrice extracellulaire par la réaction de Maillard dans le vieillissement et le diabète : le point sur "un puzzle en voie de résolution". Ann NY Acad Sci. Juin 2005 ; 1043 : 533-44.
138. Bailey AJ, Paul RG, Knott L. Mécanismes de maturation et de vieillissement du collagène. Développeur Mech Aging. 1er décembre 1998 ; 106(1-2) :1-56.
139. Bhattacharya SK, Bhattacharya A, Sairam K, Ghosal S. Effet des principes tannoïdes bioactifs d'Emblica officinalis sur le stress oxydatif induit par l'ischémie-reperfusion dans le cœur de rat. Phytomédecine. mars 2002;9(2):171-4.
140. Anila L, Vijayalakshmi NR. Effets bénéfiques des flavonoïdes de Sesamum indicum, Emblica officinalis et Momordica charantia. Phytother Rés. décembre 2000;14(8):592-5.
141. Kim HJ, Yokozawa T, Kim HY et al. Influence de l'amla (Emblica officinalis Gaertn.) sur l'hypercholestérolémie et la peroxydation lipidique chez les rats nourris avec du cholestérol. J Nutr Sci Vitaminol (Tokyo). décembre 2005;51(6):413-8.
142. Ali R, Alexander KP. Statines pour la prévention primaire des événements cardiovasculaires chez les personnes âgées : une revue des données probantes. Suis J Geriatr Pharmacother. mars 2007;5(1):52-63.
143. Doncheva NI, Nikolov KV, Vassileva DP. Effets lipidiques et pléiotropes du gemfibrozil, de la simvastatine et de la pravastatine chez les patients atteints de dyslipidémie. Folia Med (Plovdiv). 2006;48(3-4):56-61.
144. Nissen SE, Nicholls SJ, Wolski K et al. Effets d'un agoniste PPAR-alpha puissant et sélectif chez les patients atteints de dyslipidémie athérogène ou d'hypercholestérolémie : deux essais contrôlés randomisés. JAMA. 28 mars 2007; 297(12):1362-73.
145. Duan W, Yu Y, Zhang L. Effets antiathérogènes du phyllanthus emblica associés à la corilagin et à son analogue. Yakugaku Zasshi. Juillet 2005;125(7):587-91.
146. Cai X. Régulation des cellules musculaires lisses dans le développement et les maladies vasculaires : stratégies thérapeutiques actuelles. Expert Rév Cardiovasc Ther. 2006 novembre;4(6):789-800.
147. Lembo G, Vecchione C, Morisco C et al. Hypertension artérielle et athérosclérose : leur épidémiologie et physiopathologie. Ann Ital Med Int. 10 octobre 1995 (Suppl) : 69S-72S.
148. Jacob A, Pandey M, Kapoor S, Saroja R. Effet de la groseille indienne (amla) sur les taux de cholestérol sérique chez les hommes âgés de 35 à 55 ans. Eur J Clin Nutr. 1988 novembre ; 42(11) : 939-44.
149. Antony B, Benny M, Kaimal TNB. Une étude clinique pilote pour évaluer l'effet de l'extrait d'Emblica officinalis (Amlamax®) sur les marqueurs de l'inflammation systémique et de la dyslipidémie. Indien J Clin Biochem. 2008 ; 23(4):378-81.
150. Laboratoire de R&D, Arjuna Natural Extracts Ltd PBNO 126 Alwaya Cohin Karala Inde. Étude non publiée sur Amlamax®.
151. Cucuianu M, Coca M, Hancu N. Transport inverse du cholestérol et athérosclérose. Une mini revue. Rom J Intern Med. 2007;45(1):17-27.
152. Rainwater DL, Rutherford S, Dyer TD et coll. Déterminants de la variation de l'activité paraoxonase sérique humaine. Hérédité. 29 octobre 2008.
153. Rajak S, Banerjee SK, Sood S et al. Emblica officinalis provoque une adaptation myocardique et protège contre le stress oxydatif en cas de lésion ischémique-reperfusion chez le rat. Phytother Rés. 2004 janvier ; 18(1) :54-60.
154. Yoshida H, Ishikawa T, Hosoai H et al. Effet inhibiteur des flavonoïdes du thé sur la capacité des cellules à oxyder les lipoprotéines de basse densité. Biochem Pharmacol. 1er décembre 1999;58(11):1695-703.
155. Holvoet P. Relations entre le syndrome métabolique, le stress oxydatif et l'inflammation et les maladies cardiovasculaires. Verh K Acad Geneeskd Belg. 2008;70(3):193-219.
156. Lindberg G, Rastam L, Nilsson-Ehle P et al. Acide sialique sérique et sialoglycoprotéines dans l'athérosclérose asymptomatique de l'artère carotide. Enquêteurs de l'ARIC. Risque d'athérosclérose dans les communautés. Athérosclérose. Septembre 1999 ; 146(1) :65-9.
157. Moussa MA, Alsaeid M, Refai TM, et al. Association de l'acide sialique sérique avec des facteurs de risque métaboliques cardiovasculaires chez les enfants et adolescents koweïtiens atteints de diabète de type 1. Métabolisme. Mai 2004;53(5):638-43
158. Coylewright M, Blumenthal RS, Post W. Placer COURAGE dans son contexte : une revue de la littérature récente sur la gestion des maladies coronariennes stables. Mayo Clin Proc. juillet 2008;83(7):799-805.
159. Kapetanakis EI, Medlam DA, Boyce SW et al. Administration de clopidogrel avant un pontage aorto-coronarien : la panacée du cardiologue ou le casse-tête du chirurgien ? Eur Heart J. 2005 mars;26(6):576-83.
160. Shafiq N, Malhotra S, Pandhi P, Grover A. La merveille du monde « Statinthe : une panacée pour toutes les maladies ou une bulle sur le point d'éclater. J Résultats négatifs Biomed. 23 mars 2005 ; 4 : 3.
161. Czyz M, Watala C. L'aspirine "la panacée prodigieuse ? Mécanismes moléculaires de l'action de l'acide acétylsalicylique dans l'organisme. Postepy Hig Med Dosw (En ligne). 23 mars 2005 ; 59 : 105-15.
162. Lim MC. Stents à élution médicamenteuse : la panacée contre la resténose ? Singapour Med J. juillet 2004;45(7):300-2.
163. Molavi B, Rasouli N, Mehta JL. Ligands des récepteurs activés par les proliférateurs de peroxysomes comme agents antiathérogènes : panacée ou autre boîte de Pandore ? J Cardiovasc Pharmacol Ther. 2002 janvier ; 7(1) : 1-8.
164. Angiolillo DJ, Guzman LA, Bass TA. Thérapies antiplaquettaires actuelles : avantages et limites. Am Heart J. 2008 août; 156 (2 Suppl): S3-S9.
165. Derosa G, Salvadeo S, Cicéron AF. Recommandations pour le traitement de l'hypertension chez les patients atteints de diabète : évaluation critique basée sur des essais cliniques. Curr Clin.Pharmacol. 2006 janvier ;1(1):21-33.
166. El Desoky ES, Derendorf H, Klotz U. Variabilité en réponse aux médicaments cardiovasculaires. Curr Clin Pharmacol. 2006 janvier ;1(1):35-46.
167. Scartezzini P, Speroni E. Revue de certaines plantes de médecine traditionnelle indienne à activité antioxydante. J Ethnopharmacol. Juillet 2000;71(1-2):23-43.
168. Satiavati GV. L'héritage de Caraka (Critique de livre). Science actuelle. 2003;85 : 1087-90.
169. Muruganandam AV, Kumar V, Bhattacharya SK. Effet de la formulation à base de plantes, EuMil, sur les perturbations homéostatiques chroniques induites par le stress chez le rat. Indien J Exp Biol. 2002 octobre ; 40(10) : 1151-60.
* Reviews & Success Stories Disclaimer
Product reviews solely reflect the views and opinions expressed by the contributors and not those of Z Natural Foods. Z Natural Foods does not verify or endorse any claims made in these reviews. Statements have not been evaluated by the FDA and are not intended to diagnose, treat, cure, or prevent any disease or health condition.PROGRAMME DE RÉFÉRENCE
Partagez votre lien personnel avec vos amis et accueillez-les avec des récompenses. Réclamez le vôtre lors de leur premier achat.
DONNER
10 $ de réduction

OBTENIR
10 $ de réduction